Fowler S.P. et al. (2023)
Verhogen light drank en aspartaam tijdens de zwangerschap het risico op een kind met autisme?
Nutrients . 2023 Aug 29;15(17):3772. doi: 10.3390/nu15173772.
Soort onderzoek: Patiënt-control-onderzoek
Een studie, gepubliceerd in augustus 2023, laat een verband zien tussen het gebruik van light drank en aspartaam tijdens de zwangerschap en/of het geven van borstvoeding en een verhoogd risico op het krijgen van een zoon met autisme [1]. Is dat aanleiding voor zwangere vrouwen om geen light drank en aspartaam meer te gebruiken? Nee, dat kan niet geconcludeerd worden uit die studie.
Wat is de aanleiding en hoofdvraag van de onderzoekers?
De laatste decennia wordt steeds vaker de diagnose autisme gesteld (zie blauwe kader). In Amerika was dat voor 1980 minder dan 0,03% van de kinderen, wat gestegen is tot 2,8% in 2020. Er zijn geen officiële Nederlandse cijfers, maar op basis van internatonale literatuur wordt geschat dat bij ons 1% van de kinderen en volwassenen autisme heeft [1]. Redenen voor deze toename zijn veranderingen van de definitie voor het stellen van de diagnose, meer testen en meer geld beschikbaar voor het onderwerp autisme, naast mogelijk veranderingen in eetpatroon, omgeving en andere factoren die de omgeving in de baarmoeder van zwangere vrouwen beïnvloeden.
De voedingstoestand van een zwangere vrouw met een voldoende inname van belangrijke voedingsstoffen lijkt de kans op het krijgen van een kind met autisme te verkleinen [2]. Daarentegen is er een theorie dat methanol en aspartaam de kans erop verhogen [3]. Om dat dit verder te onderzoeken hebben wetenschappers gekeken of er een verband is tussen de inname van light frisdrank en aspartaam tijdens de zwangerschap en/of het geven van borstvoeding en het krijgen van een kind met autisme [4].

Welke onderzoeksmethode is gebruikt?
De studie die is uitgevoerd heette de ‘Autism Tooth Fairy Study’ (ATFS) en vond plaats in Amerika tussen 2011 en 2014. Daarvoor zijn 356 kinderen gerekruteerd die tussen 1984 en 2011 waren geboren. Een deel daarvan had autisme (n=235) en een ander deel niet (n=121) wat de controlegroep was. Aan de moeders werd gevraagd om vragenlijsten in te vullen over zichzelf, hun eetpatroon, hun kind, de gezinssituatie, etc. in de periode dat ze zwanger waren en/of borstvoeding gaven. Er werd onder andere gevraagd hoe vaak ze light drank dronken en hoe vaak ze zoetstoffen hadden gebruikt in hun koffie, thee etc. Omdat naar specifieke merken werd gevraagd kon de inname van aspartaam worden geschat.
Vervolgens is er gekeken naar moeders die a) meer of minder dan 350 ml (volume van een blikje in Amerika) per dag hadden gedronken en b) meer of minder dan 177 mg aspartaam per dag hadden binnengekregen (ongeveer de hoeveelheid aspartaam in één blikje). Dit soort onderzoek heet een patiënt-control-onderzoek waarin wordt teruggekeken in de tijd (retrospectief). Wat betreft het vaststellen van autisme zijn er twee definities gebruikt (zie blauwe kader boven):
- Klassiek autisme
- Autismespectrumstoornis
Bij die twee definities is er vervolgens ook nog in een subanalyse gekeken naar kinderen zonder regressieve vorm. Regressief autisme is een vorm van autisme waarbij een kind zich normaal lijkt te ontwikkelen, maar plotseling de spraak- en sociale vaardigheden begint te verliezen. Dit is allemaal uitgesplitst naar zoons, dochters en zoons + dochters.
In de analyse werd er gecorrigeerd voor verschillen in identiteit van de moeder, wervingsbron, etniciteit van het kind (niet-Spaans blank versus anders), geboortejaar, opleiding van de moeder (≥4 jaar universiteit versus lager) en het inkomen van het huishouden (≥USD 100.000/jaar versus minder).
Wat is de bewijskracht van de gekozen onderzoeksmethode?
De gebruikte ondersmethode is een patiënt-controle-onderzoek. Dat is een retrospectieve onderzoeksmethode (terugkijken in de tijd). Uitgangspunt is deelnemers met de ziekte (ouders van kinderen met autisme), waar vervolgens risicofactoren bij gezocht worden door ze te vergelijken met deelnemers zonder die ziekte (ouders van kinderen zonder autisme), de controlegroep. Deze onderzoeksmethode is geschikt voor de bestudering van zeldzame aandoeningen omdat niet gewacht hoeft te worden totdat het aantal gewenste deelnemers de zeldzame aandoening heeft gekregen.
De bewijskracht van deze onderzoeksmethode is laag door verschillende tekortkomingen. Lager dan de observationele cohortstudies waarin deelnemers in de tijd gevolgd worden (zie figuur). Zo is er teruggekeken in de tijd toen de moeders nog zwanger waren en borstvoeding gaven. Dan moet er aanspraak worden gemaakt op het geheugen van de moeders waardoor (onbewust) fouten kunnen worden gemaakt. Het kan ook zijn dat de moeders van autistische kinderen zich bepaalde dingen beter of anders herinneringen dan de moeders van kinderen zonder autisme. Verder is het een observationele opzet, zonder interventie, waardoor verstorende factoren een rol kunnen spelen. Er kan daarom niet gesproken worden van een oorzaak-gevolgrelatie.
Tegenover een patiënt-controle-onderzoek staat het gerandomiseerd, dubbelblind, gecontroleerd onderzoek (zie figuur). Dit soort onderzoek wordt als de gouden standaard gezien. Hierin wordt een groep met vergelijkbare deelnemers in twee of meerdere groepen verdeeld. Het enige wat anders is, is de interventie die ze gedurende een bepaalde tijd volgen (bijvoorbeeld wel of geen light drank drinken). De verschillen in uitkomst moeten dan door de betreffende interventie veroorzaakt zijn.
Figuur: Piramide van bewijslast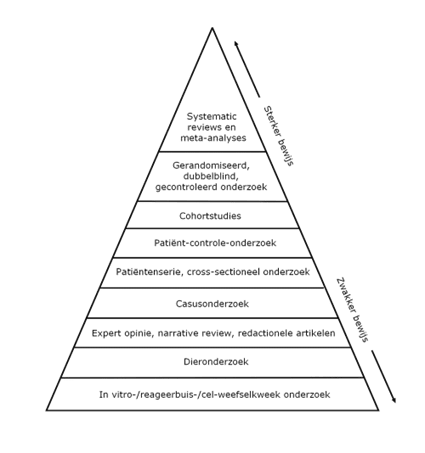
Welke resultaten zijn er gevonden?
Zoons
Moeders die ≥350 ml light drank per dag dronken hadden een 3,1 keer verhoogd risico op het krijgen van een zoon met klassiek autisme. Voor klassiek autisme zonder regressie werd een 3,5 keer verhoogd risico gevonden. Er werd geen verhoogd risico gevonden op het krijgen van een zoon met een autismespectrumstoornis, ook niet zonder regressie (zie tabel 1).
Moeders die tijdens die ≥177 mg aspartaam per dag binnenkregen hadden een 3,4 keer verhoogd risico op het krijgen van een zoon met klassiek autisme. Voor klassiek autisme zonder regressie werd een 3,7 keer verhoogd risico gevonden. Er werd geen verhoogd risico gevonden op het krijgen van een zoon met een autismespectrumstoornis, ook niet zonder regressie (zie tabel 2).
Dochters
Moeders die ≥350 ml light drank per dag hadden dronken of ≥177 mg aspartaam per dag binnenkregen, hadden geen verhoogd risico op het krijgen van een dochter met klassiek autisme of een autismespectrumstoornis (zie tabellen 1 en 2).
Zoons + dochters
Moeders die ≥ 350 ml light drank per dag dronken of ≥177 mg aspartaam per dag binnenkregen hadden geen verhoogd risico op het krijgen van een kind (zoon + dochter) met klassiek autisme of een autismespectrumstoornis (zie tabellen 1 en 2).
Autismevorm | Zoon | Dochter | Zoon + dochter |
Autismespectrumstoornis
| ↔ | ↔ | ↔ |
Autismespectrumstoornis zonder regressie | ↔ | ↔ | ↔ |
Klassiek autisme
| 3,1 x ↑ | ↔ | ↔ |
Klassiek autisme zonder regressie | 3,5 x ↑ | ↔ | ↔ |
Tabel 1: Het drinken van light drank (≥350 ml/dag) tijdens de zwangerschap en/of het geven van borstvoeding en het risico op het krijgen van een kind met verschillende vormen van autisme.
Autismevorm | Zoon | Dochter | Zoon + dochter |
Autismespectrumstoornis
| ↔ | ↔ | ↔ |
Autismespectrumstoornis zonder regressie | ↔ | ↔ | ↔ |
Klassiek autisme
| 3,4 x ↑ | ↔ | ↔ |
Klassiek autisme zonder regressie | 3,7 x ↑ | ↔ | ↔ |
Tabel 2: Het binnenkrijgen van aspartaam (≥177 mg/dag) tijdens de zwangerschap en/of het geven van borstvoeding en het risico op het krijgen van een kind met verschillende vormen van autisme.
Wat zijn de conclusies van de onderzoekers?
De auteurs geven aan dat, zoals de resultaten laten zien, het drinken van light drank en het gebruik van aspartaam tijdens de zwangerschap en/of het geven van borstvoeding het risico op het krijgen van een zoon met autisme verhoogt. Ze merken daarbij op dat er geen bewijs is voor een oorzakelijk verband, maar dat het, in combinatie met eerdere bevindingen uit dierstudies, wel nieuwe zorgen geeft over het gebruik van light drank en aspartaam tijdens de zwangerschap. Meer en beter onderzoek is nodig om meer duidelijkheid te krijgen.
Wat zijn de sterke punten van de studie?
- Patiënt-controle-studies zijn relatief goedkoop en worden vaak gebruikt als één van de eerste studies die aanwijzingen kunnen leveren voor een verband tussen blootstelling aan een voedingsmiddel of voedingsstof en een gezondheidsprobleem of ziekte. Dit is ook één zo’n studie.
Wat zijn de zwakke punten van de studie?
- De gebruikte onderzoeksmethode (patient-controle-onderzoek) heeft een lage bewijskracht.
- De vragen gingen over het eetpatroon van verschillende jaren geleden toen ze zwanger waren en/of borstvoeding gaven. Mogelijk tot 29 jaar geleden wanneer het kind in 1985 geboren is en de moeder in 2014 de vragenlijst had ingevuld. Dat zal ongetwijfeld tot fouten hebben geleid omdat bepaalde dingen niet meer, of verkeerd herinnerd worden.
- De moeders met een kind met autisme hebben de vragen over hun vroegere eetpatroon ingevuld met de wetenschap dat ze nu een kind hebben met autisme. Dat kan invloed hebben gehad op de antwoorden. Bij de controlegroep speelt dit niet.
- De antwoorden waren gebaseerd op zelfrapportage.
- Er is niet gekeken of de moeders tijdens hun zwangerschap last hadden van overgewicht/obesitas, diabetes type 2 en geestelijke gezondheidsproblemen omdat die gegevens ontbtaken. Dat kan wel factoren die invloed hebben op het krijgen van een kind met autisme [5, 6]. Juist mensen die te zwaar zijn (80% van de mensen met diabetes type 2 is te zwaar) gebruiken light drank en aspartaam om daar iets aan te doen. Het zou dan het hebben van overgewicht/obesitas tijdens de zwangerschap geweest kunnen zijn dat het risico op een zoon met autisme heeft verhoogd en niet het drinken van light drank of het gebruik van aspartaam.
- Er waren geen gegevens beschikbaar over het eetpatroon van de vaders tijdens de preconceptuele periode.
- Bij de berekening van de aspartaam-inname is naar drie bronnen gekeken: light frisdrank, andere light dranken en zakjes met zoetstoffen (tafelzoetstof). Aangezien aspartaam ook in andere voedingsmiddelen zit zal dit de minimale inname zijn en zal de werkelijke inname van de moeders hoger zijn geweest. Het is dan mogelijk dat moeders die nu in de controlegroep zaten toch meer dan 177 mg aspartaam binnenkregen.
- Het is opmerkelijk dat alleen bij de moeders met een zoon een verhoogd risico werd gevonden en dan alleen op klassiek autisme. Dat zet vraagtekens bij wat het vermeende werkingsmechanisme zou moeten zijn. Wanneer light drank en aspartaam tijdens de zwangerschap en/of het geven van borstvoeding een ongunstig effect zouden hebben op de sociale communicatie en gedragspatronen van kind, waarom dan alleen bij de zoontjes en op klassiek autisme?
- Het aantal deelnemers was klein. Ook was het aantal kinderen in de controlegroep klein in verhouding tot het aantal kinderen met autisme, met name bij moeders met een zoon (zie tabel 3). Dat zou de resultaten kunnen hebben beïnvloed. Wanneer het aantal deelnemers groter wordt neemt de kans namelijk toe dat je een statistisch significant effect vindt.
| Autismespectrum- stoornis | Klassiek autisme | Klassiek autisme zonder regressie | Controlegroep |
Zoon | 203 | 140 | 86 | 54 |
Dochter | 32 | 28 | 19 | 67 |
Tabel 3: Aantal kinderen met autisme en zonder autisme (controlegroep) naar geslacht.
Wat betekent deze studie voor het drinken van light dranken of het gebruik van aspartaam tijdens de zwangerschap?
Deze studie heeft veel beperkingen en kan door de opzet geen oorzaak-gevolg-relatie aantonen. Daarnaast heeft de EFSA geconcludeerd dat er geen bewijs is dat aspartaam een effect heeft op het gedrag en cognitief functioneren bij kinderen en volwassenen. Dat betekent dat er geen aanleiding is om tijdens de zwangerschap en/of het geven van borstvoeding geen light drank of aspartaam te gebruiken.
Referenties
- GGZ. Zorgstandaard autism. 2017.
- Zhong C, Tessing J, Lee BK, Lyall K. Maternal Dietary Factors and the Risk of Autism Spectrum Disorders: A Systematic Review of Existing Evidence. Autism Res. 2020 Oct;13(10):1634-1658.
- Walton RG, Monte WC. Dietary methanol and autism. Med Hypotheses. 2015 Oct;85(4):441-6.
- Fowler SP, Gimeno Ruiz de Porras D, Swartz MD, Stigler Granados P, Heilbrun LP, Palmer RF. Daily Early-Life Exposures to Diet Soda and Aspartame Are Associated with Autism in Males: A Case-Control Study. Nutrients. 2023 Aug 29;15(17):3772.
- Lei XY, Li YJ, Ou JJ, Li YM. Association between parental body mass index and autism spectrum disorder: a systematic review and meta-analysis. Eur Child Adolesc Psychiatry. 2019 Jul;28(7):933-947.
- Wan H, Zhang C, Li H, Luan S, Liu C. Association of maternal diabetes with autism spectrum disorders in offspring: A systemic review and meta-analysis. Medicine (Baltimore). 2018 Jan;97(2):e9438.
- Abdel-Salam OM, Salem NA, El-Shamarka ME, Hussein JS, Ahmed NA, El-Nagar ME. Studies on the effects of aspartame on memory and oxidative stress in brain of mice. Eur Rev Med Pharmacol Sci. 2012 Dec;16(15):2092-101.
- Abu-Taweel GM, A ZM, Ajarem JS, Ahmad M. Cognitive and biochemical effects of monosodium glutamate and aspartame, administered individually and in combination in male albino mice. Neurotoxicol Teratol. 2014 Mar-Apr;42:60-7.
- Onaolapo AY, Onaolapo OJ, Nwoha PU. Alterations in behaviour, cerebral cortical morphology and cerebral oxidative stress markers following aspartame ingestion. J Chem Neuroanat. 2016 Dec;78:42-56.
- Jones SK, McCarthy DM, Vied C, Stanwood GD, Schatschneider C, Bhide PG. Transgenerational transmission of aspartame-induced anxiety and changes in glutamate-GABA signaling and gene expression in the amygdala. Proc Natl Acad Sci U S A. 2022 Dec 6;119(49):e2213120119.
- Jones SK, McCarthy DM, Stanwood GD, Schatschneider C, Bhide PG. Learning and memory deficits produced by aspartame are heritable via the paternal lineage. Sci Rep. 2023 Aug 31;13(1):14326.
- Villareal LMA, Cruz RAM, Ples MB, Vitor RJS. Neurotropic effects of aspartame, stevia and sucralose on memory retention and on the histology of the hippocampus of the ICR mice (Mus musculus). Asian Pacific Journal of Tropical Biomedicine, Volume 6, Issue 2, 2016,Pages 114-118, ISSN 2221-1691.
- EFSA ANS Panel (EFSA Panel on Food Additives and Nutrient Sources added to Food), 2013. Scientific Opinion on the re-evaluation of aspartame (E 951) as a food additive. EFSA Journal 2013;11(12):3496, 263 pp.
Lees publicatie op
https://pubmed.ncbi.nlm.nih.gov/37686804/